Cotidiano
Covid-19: Brasil recebe mais 1,5 milhão de doses de vacina da Pfizer
Tweet
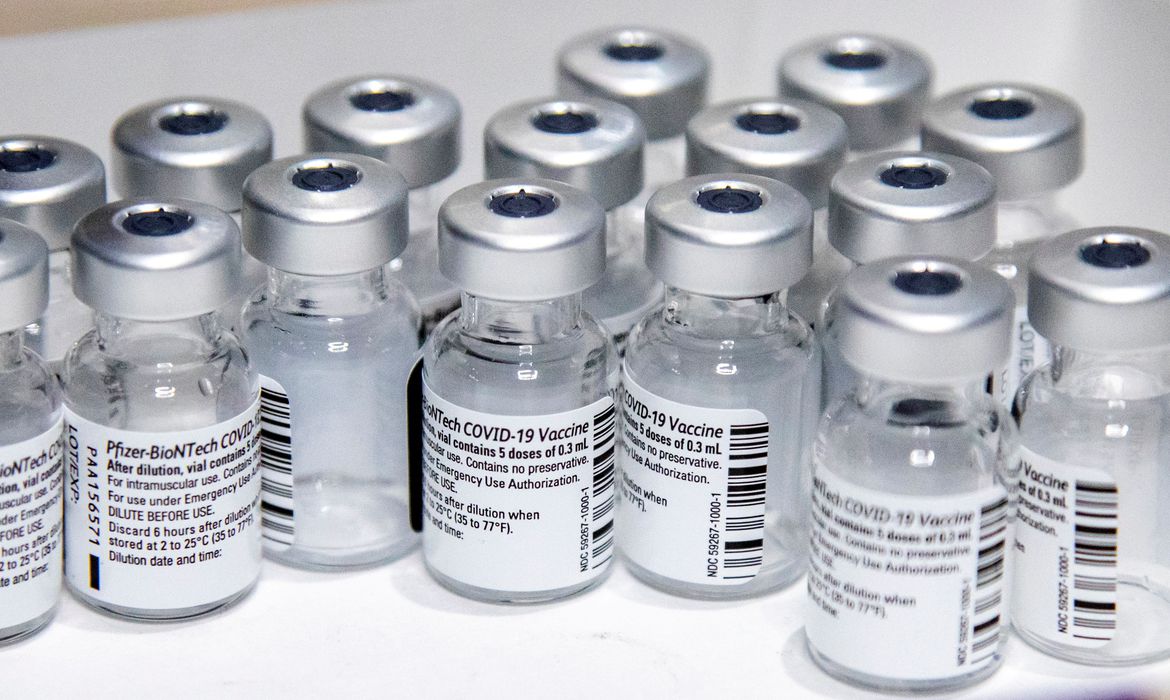
Um avião com um novo carregamento de vacinas ComiRNaty, da Pfizer/BioNTech, pousou por volta das 14h deste sábado (4) no Aeroporto de Viracopos, em Campinas, interior de São Paulo. Segundo a Pfizer, composto por 1,52 milhão de doses, este foi o 63º lote de vacinas contra a covid-19 enviado ao Brasil.
O imunizante da Pfizer é aplicado em duas doses.
A chegada deste lote ao Brasil estava prevista para a sexta-feira (3), mas, segundo a Pfizer, por questões logísticas, o voo foi remanejado para hoje.
O Ministério da Saúde informou que a distribuição dessas doses ocorrerá nos próximos dias. Desde o início da campanha de vacinação contra a covid-19, no Brasil, o ministério informa já ter distribuído aos estados e ao Distrito Federal mais de 55,2 milhões de doses da vacina da Pfizer/BioNTech.
De acordo com o ministério, mais de 253,7 milhões de doses de vacinas contra a covid-19 já foram destinadas a todo o Brasil. Isso inclui as vacinas da Pfizer/BioNTech, AstraZeneca/Oxford/Fiocruz e CoronaVac/Butantan/Sinovac, que são aplicadas em duas doses, e a Janssen, que é aplicada em dose única.
Ainda segundo o ministério, mais de 133,5 milhões de brasileiros receberam ao menos a primeira dose e 65,6 milhões estão completamente imunizados com as duas doses ou a dose única.
Fonte: Agência Brasil
CoronaVac: Anvisa veta 21 milhões de doses envasadas em local sem inspeção

A Anvisa determinou hoje a suspensão de forma cautelar de ao menos 25 lotes da vacina CoronaVac envasados em local não autorizado pela agência. No total, a decisão afeta 21 milhões de doses, sendo 12 milhões já recebidas pelo Instituto Butantan e outras 9 milhões em processo de envio ao Brasil.
A Anvisa informou que o Instituto Butantan comunicou ontem que a Sinovac, fabricante da vacina, "enviou ao Brasil 25 lotes na apresentação frasco-ampola, totalizando 12.113.934 doses". No entanto, a unidade responsável pelo envase não foi aprovada na inspeção da Anvisa durante a Autorização de Uso Emergencial do imunizante.
"O Instituto informou ainda que outros 17 lotes, também envasados no local não inspecionado pela Anvisa, totalizando 9.000.000 de doses, estão em tramitação de envio e liberação ao Brasil."
Como o local do envase não foi aprovado na Autorização de Uso Emergencial, a Anvisa informou que o produto não é considerado regularizado pela agência. A decisão foi publicada esta tarde em Edição Extra do Diário Oficial da União.
"A Anvisa avaliou toda a documentação apresentada pelo Instituto Butantan, consultou as bases de dados internacionais em busca de informações acerca das condições de boas práticas de fabricação da empresa responsável pelo envase desses lotes e até o momento não localizou nenhum relatório de inspeção emitido por outras autoridades de referência, como por exemplo PIC/S e OMS, ou emitido pela própria Anvisa", informou.
E acrescenta: "considerando a irregularidade apontada, somado às características do produto e complexidade do processo fabril, devendo ser fabricadas em rigorosas condições assépticas, e o desconhecimento sobre o cumprimento das boas práticas de fabricação da empresa pela Anvisa, indicam a necessidade de adoção de medida cautelar para evitar a exposição da população a possível risco iminente."
Os lotes impactados podem ser consultados no site da agência.
A Anvisa esclarece que a medida é cautelar e não uma decisão condenatória em caráter punitivo, "mas sim, medidas sanitárias para evitar a exposição ao consumo e uso de produtos irregulares ou sob suspeita."
A agência informou que serão feitas tratativas junto ao Butantan para a regularização do novo local na cadeia fabril da vacina.
Butantan descarta risco
Em nota enviada ao UOL, o Instituto Butantan disse que a medida da Anvisa não deve causar alarmismo, pois "foi o próprio Instituto que, por compromisso com a transparência e por extrema precaução, comunicou o fato à agência, após atestar a qualidade das doses recebidas. Isso garante que os imunizantes são seguros para a população."
O instituto diz ainda ter convicção de que a certificação deve ser concedida em breve pela Anvisa, pois diz ter enviado "há 15 dias toda a documentação necessária para a certificação do processo de produção em que foram feitas essas doses". O órgão se colocou a disposição para fornecer mais dados, se a Anvisa julgar necessário.
"Todos os lotes liberados pelo instituto estão de posse do Ministério da Saúde, como firmado em contrato", informou. "Reafirmamos, no entanto, que todas as doses que saíram da unidade fabril estão atestadas pelo rigoroso controle de qualidade do Butantan."
"Informa, ainda, que 6 milhões de doses da vacina do Butantan, que fazem parte de um lote de 12 milhões de imunizantes formuladas no site fabril da zona oeste de SP, aguardavam liberação da Anvisa. Na última quinta-feira (2), o órgão regulatório liberou e as mesmas foram expedidas na sexta-feira (3)."
E acrescenta: "Esse pedido de liberação ao órgão regulatório aconteceu por uma mudança em uma das etapas do processo de formulação da vacina, que pode ocorrer no decorrer da fabricação. A fábrica onde é feita a formulação e o envase da CoronaVac são todas certificadas pela Anvisa, desde o final de 2020."
O instituto finaliza a nota convidando a Anvisa para voltar a conhecer as instalações das fábricas da Sinovac, na China.
Fonte: UOL