Cotidiano
Anvisa autoriza vacina da Pfizer contra covid-19 em crianças
Tweet
Poderão ser vacinadas crianças com idade de 5 a 11 anos
A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou o uso da vacina produzida pelo consórcio Pfizer-BioNTech, a Comirnaty, contra a covid-19 em crianças com idade de 5 a 11 anos.
A aprovação foi anunciada hoje (16), em transmissão ao vivo da Anvisa, no Youtube, após avaliação técnica da agência, sobre o pedido apresentado em novembro, indicando o uso da vacina para este público. A resolução com a autorização da Anvisa será publicada ainda hoje (16) no Diário Oficial da União, em edição especial, segundo gerente geral de Medicamentos da Anvisa, Gustavo Mendes.Gustavo Mendes.
“Com base na totalidade das evidências científicas disponíveis, a vacina Pfizer-BioNTech, quando administrada no esquema de duas doses em crianças de 5 a 11 anos de idade, pode ser eficaz na prevenção de doenças graves, potencialmente fatais ou condições que podem ser causadas pelo SARS-CoV-2”, disse Mendes.
O gerente lembrou que as análises contaram com a participação de diversos especialistas tanto da Anvisa como de outras entidades. “Verificamos segurança e tolerabilidade, em uma primeira fase. Nela foram aplicadas doses diferentes. Com base no resultado, chegamos à conclusão de que deveriam ser aplicadas 10 microgramas, quantidade inferior à aplicada em adultos”, disse.
Ele acrescentou que, na comparação entre crianças de 5 a 11 com pessoas de 16 a 25 anos [considerando as doses correspondentes a cada grupo], foi identificada a presença de anticorpos nas crianças.
“Observamos desempenho satisfatório da vacina também contra a variante Delta”, ressaltou. “E não há relato de nenhum evento adverso sério, de preocupação ou relato relacionado a casos muito graves ou mortalidade por conta da vacinação. Esse perfil de segurança é muito importante”, completou.
De acordo com a gerente geral de Monitoramento, Suzie Marie Gomes, as doses de vacinas para crianças é de um terço em relação à dose e à formulação aprovada anteriormente. Além disso a formulação pediátrica é diferente. Ou seja, não se pode fazer diluição da dose de adulto para a dose de criança.
Suzie Marie acrescenta que as crianças que completarem 12 anos entre a primeira e a segunda dose devem manter a dose pediátrica. A vacina da Pfizer-BioNTech já havia sido autorizada para aplicação em adolescentes com idade a partir de 12 anos.
Por fim, a gerente de Monitoramento ressalta que não há estudos sobre coadministração com outras vacinas e que, portanto, o uso de diferentes vacina não é indicado.
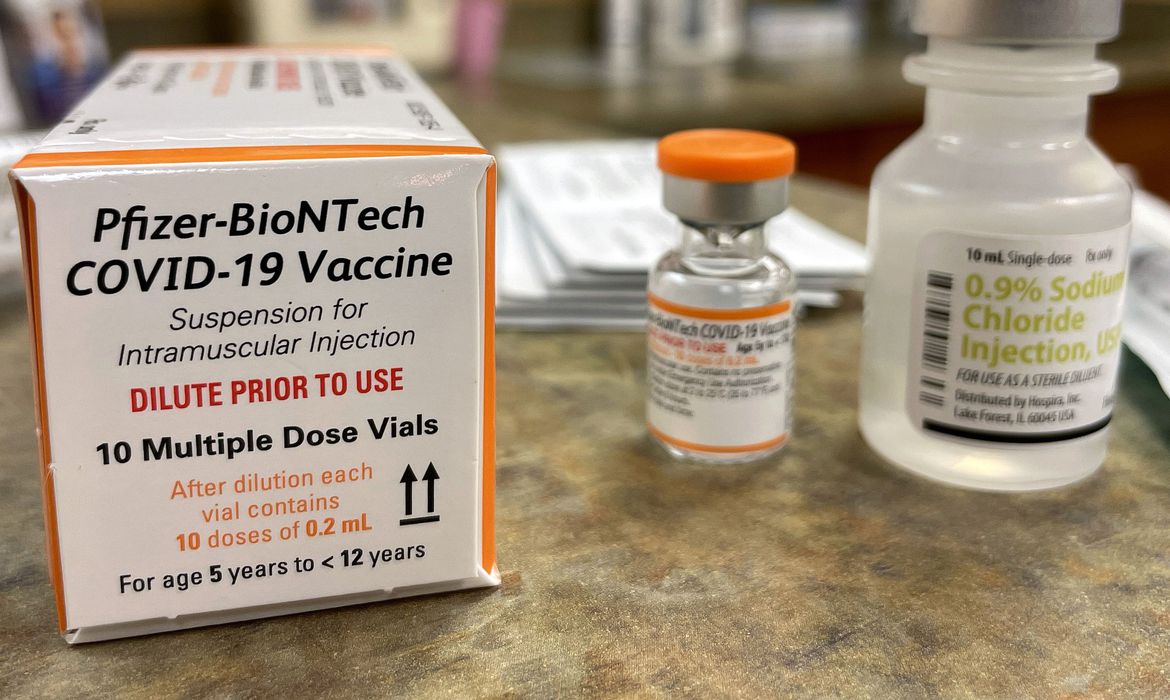
Segundo a Anvisa, a dose da vacina para crianças será diferente daquela utilizada para pessoas a partir de 12 anos. Os frascos também terão cores distintas para evitar erros na aplicação.
Confira outras notícias
- Anvisa faz recomendações para uso de vacina da Pfizer em crianças
Após autorizar o uso da vacina da Pfizer em crianças com idade entre 5 e 11 anos, a Agência Nacional de Vigilância Sanitária (Anvisa) apresentou hoje (16) algumas recomendações e condições que devem ser observadas pelas autoridades de saúde para a imunização desse público. De acordo com a agência, a atenção deve ser redobrada uma vez que tanto a dose como a formulação da vacina a ser aplicada serão diferentes das aplicadas em jovens e adultos.

A exemplo do que ocorreu nos demais grupos, a vacinação em crianças deve priorizar grupos consideradas como de risco. Um ponto muito importante, ressaltado pela diretora da Anvisa e relatora do processo de liberação do medicamento, Meiruze Sousa Freitas, é que pais ou responsáveis fiquem atentos com relação ao frasco da vacina, que terá cor laranja. Para adultos, o frasco é roxo.
A administração da vacina em crianças será de duas doses de 10 microgramas com três semanas de intervalo. “O volume a ser aplicado é de 0,2 ml em uma seringa de 1 ml”, explicou a diretora.
Recomendações
Meiruze lembrou que caberá ao Ministério da Saúde a decisão sobre “conveniência e oportunidade” para inclusão da vacina no Programa Nacional de Imunização, mas que cabe à Anvisa apresentar as recomendações e condições que devem ser seguidas para a vacinação das crianças nessa faixa etária.
“A vacinação das crianças nessa faixa etária deve ser iniciada após treinamento completo das equipes que de saúde que farão a aplicação, uma vez que a grande maioria dos eventos adversos pós-vacinação é decorrente da administração do produto errado a faixas etárias erradas, de doses inadequadas e da preparação errônea do produto”, disse a diretora.
Uma outra recomendação da Anvisa é de que a vacinação das crianças seja feita em “ambiente específico e segregado da vacinação de adultos”. O ambiente deve ser “acolhedor e seguro para a população pediátrica”. É também indicado que as crianças permaneçam no local em que a vacinação ocorrer por pelo menos 20 minutos após a aplicação, de forma a serem observadas por esse período.
A sala em que se dará a aplicação da vacina deve ser exclusiva para a aplicação dessa vacina. E não deve ser aproveitada para a aplicação de outras vacinas, ainda que pediátricas. Não havendo essa possibilidade na infraestrutura, para essa aplicação, que sejam adotadas todos cuidados visando uma administração segura.
No caso de comunidades isoladas, como aldeias indígenas, a Anvisa recomenda que, sempre que possível, a vacina seja feita em dias separados, não coincidentes com os dias de aplicação em adultos.
Intervalo de 15 dias
Segundo a diretora da Anvisa, a vacina não deve ser administrada de forma concomitante com outras vacinas do calendário infantil. “Por precaução é recomendado intervalo de 15 dias”, disse a diretora.
A modalidade de vacinação drive thru também deve ser evitada.
Outra recomendação é que os agentes de saúde devem informar aos pais ou responsáveis que acompanham crianças e adolescentes sobre sintomas e reações esperadas após a vacinação, como dor, inchaço ou vermelhidão local, febre, fadiga, dor de cabeça ou linfadenopatia (gânglios) na axila do braço que recebeu a vacina.
“Pais ou responsáveis devem procurar um médico, caso a criança apresente dores repentinas no peito, falta de ar ou palpitações após a aplicação da vacina”, afirmou a diretora. Crianças que completarem 12 no intervalo entre a primeira e a segunda dose deverão manter a dose pediátrica.
Secretários de Saúde
O Conselho Nacional de Secretários de Saúde (Conass) divulgou nota na qual manifestou apoio à aprovação do imunizante para esse público. Nela, o presidente da entidade, Carlos Lula, destaca que o imunizante já foi aprovado para a faixa etária pela Agência Europeia de Medicamentos (EMA), pela Agência Americana Food and Drug Administration (FDA) e pelo governo de Israel.
“Tendo em vista que para dar início à vacinação nesta faixa etária será necessária formulação específica desta vacina com um terço da fórmula padrão [10 microgramas por dose], o Conass aguarda posicionamento do Ministério da Saúde quanto à sua aquisição, o que é de sua competência. Aguardamos também, com expectativa, o processo de avaliação da vacina CoronaVac, do Instituto Butantan, para a vacinação de crianças e adolescentes de 5 a 17 anos, já amplamente utilizada em outros países, com disponibilidade imediata no Brasil”, disse Carlos Lula.
Contatado pela Agência Brasil, o Ministério da Saúde informou que não há, ainda, previsão sobre quando começará a aplicar a vacina da Pfizer em crianças com idade entre 5 e 11 anos.
Ameaças
O diretor presidente da Anvisa, Antônio Barra Torres, aproveitou o anúncio para denunciar que todos diretores da Anvisa receberam ameaças - algumas de morte - de pessoas contrárias à vacinação em crianças.
Segundo Torres, “o acirramento da violência anti-vacina está em viés crescente”, mas o trabalho que vem sendo desenvolvido pela agência não será prejudicado.
Ele informou que “não cabe à Anvisa e, sim, às autoridades de saúde, a aplicação do imunizante".
- Anvisa avalia novo pedido de uso da vacina CoronaVac em crianças
Solicitação do Instituto Butantan abrange público de 3 a 17 anos
A Agência Nacional de Vigilância Sanitária (Anvisa) recebeu um novo pedido do Instituto Butantan indicando a aplicação da vacina CoronaVac em crianças e adolescentes com idades entre 3 e 17 anos.
Em nota, a Anvisa explicou que, para a inclusão de “novos públicos na bula”, será necessário ao laboratório que conduza “estudos que demonstrem a relação de segurança e eficácia para determinada faixa etária”.
Prazo é de até 30 dias
“Este é o segundo pedido do laboratório para indicação do imunizante para essa faixa etária. O primeiro, apresentado em julho, foi avaliado pela Anvisa e negado devido à limitação de dados dos estudos apresentados naquele momento”, informou a Anvisa, que tem agora prazo de até 30 dias para avaliar a nova solicitação.
A Anvisa lembrou, ainda, que a vacina CoronaVac tem autorização para uso emergencial no Brasil apenas para pessoas com 18 anos de idade ou mais.
“A solicitação de ampliação de uso da vacina, ou seja, a inclusão de uma nova faixa etária, é feita pelo laboratório responsável pelo imunizante”, acrescentou a agência.
- Ministério da Saúde já tem planos para compra de vacinas para crianças
Anvisa aprovou nesta quinta-feira (16/12) o uso do imunizante da Pfizer para crianças de 5 a 11 anos. Intenção da pasta, como apurou o Correio, é incluir público-alvo na campanha de vacinação contra a covid-19
Diante da aprovação do uso da vacina contra a covid-19 da Pfizer para crianças de 5 a 11 anos, feita pela Agência Nacional de Vigilância Sanitária (Anvisa) nesta quinta (16/12), o Ministério da Saúde já tem planos para comprar doses do imunizante, que é diferente do já adquirido e utilizado no Brasil. A intenção da pasta, como apurou o Correio, é incluir este público-alvo na campanha de vacinação contra a covid-19.
A vacina da Pfizer é, a partir de hoje, a única vacina contra o coronavírus que pode ser aplicada em crianças de 5 a 11 anos no Brasil, mas, por ser diferente do imunizante da farmacêutica já comprado e aplicado no Brasil em pessoas a partir de 12 anos, é necessário que uma nova compra seja feita pelo Ministério da Saúde.
Durante a reunião que estabeleceu a aprovação da vacina da Pfizer para crianças, os técnicos da Anvisa explicaram que existem diversas diferenças entre os imunizantes da farmacêutica. Entre elas está a dosagem, menor para crianças. Além disso, as substâncias que compõem o imunizante são diferentes e até mesmo as condições para armazenamento das vacinas e os frascos são distintos.
CoronaVac
Ainda que exista a intenção do Ministério da Saúde em adquirir a vacina da Pfizer para crianças, a pasta também pode ter, em um futuro próximo, a vacina CoronaVac como opção de imunizante para crianças. Nesta quarta (15), o Instituto Butantan fez um novo pedido para que a Anvisa avalie o uso da CoronaVac em crianças e adolescentes de 3 a 17 anos.
Em agosto, a Diretoria Colegiada da Anvisa considerou, por unanimidade, não ser seguro aprovar o uso do imunizante para crianças e adolescentes "por causa da limitação de dados dos estudos apresentados naquele momento".
Mesmo sem autorização da Anvisa, o governo do estado de São Paulo já reservou 12 milhões de doses da CoronaVac com o objetivo de aplicar o imunizante em crianças de 3 a 11 anos, faixa etária que ainda não se vacinou contra a covid-19 no país.
Fonte: Agência Brasil - Correio Braziliense